FDA päivittää parhaillaan lopullisia ohjeita glukoosimittareiden ja testiliuskojen vaaditusta tarkkuudesta säätämällä hieman vuonna 2016 käyttöönotettua käytäntöä, joka kiristi näiden diabeteksen hallinnan keskeisten työkalujen valvontaa.

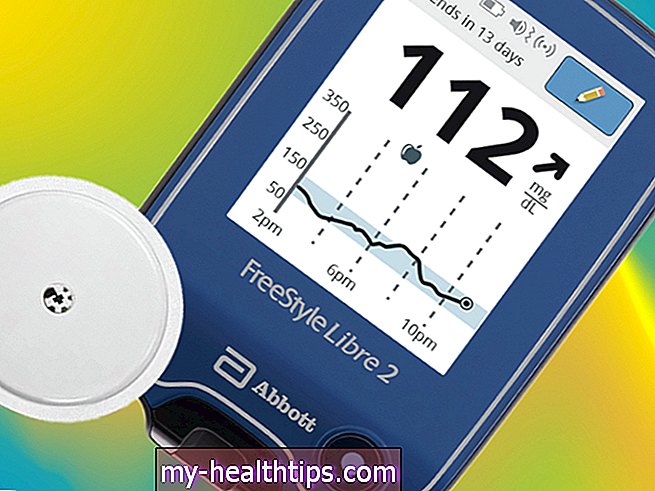
Vaikka jotkut saattavat miettiä tämän tarvetta tai merkitystä aikana, jolloin jatkuvat glukoosimonitorit (CGM) näyttävät syrjäyttävän perinteiset sormenpainemittarit, todellisuus on, että vain pieni osa PWD: stä (diabeetikoilla) käyttää CGM: ää tähän mennessä; on epärealistista ajatella, että perinteiset mittarit ja testiliuskat katoavat milloin tahansa pian. Tämä tarkoittaa, että nauhojen tarkkuus on edelleen kriittinen.
FDA julkaisi 29. marraskuuta päivitetyt ohjeet, jotka määrittelevät kliinisissä olosuhteissa käytettävien mittareiden ja henkilökohtaisen käytön mittareiden standardit. Helmikuuhun 2019 asti on avoinna julkinen kommentointijakso, jonka jälkeen virasto tarkistaa palautteen ennen kuin lopulta julkaisee virallisia, viimeisteltyjä sääntöjä.
Ne, jotka ovat seuranneet tätä asiaa vuosien varrella, saattavat kokea déjà vu -tapahtuman vastaavista keskusteluista ja ohjeiden luonnoksista, jotka julkaistiin vuoden 2004 alussa ennen lopullisten sääntöjen tuloa lokakuussa 2016. Se oli tuolloin valtava, koska tarkkuussäännöt eivät olleet muuttuneet Yhdysvalloissa 1990-luvulta lähtien!
Tärkeää on, että vuonna 2016 annettuja uusia sääntöjä sovellettiin vain uusiin tuotteisiin, eivätkä ne vaikuttaneet jo markkinoilla oleviin mittareihin ja nauhoihin. Joten vaikka nämä uudet tiukemmat tarkkuusvaatimukset olivat positiivinen muutos, D-yhteisömme oli pidettävä mielessä, että diabetesta sairastavien ihmisten käsissä oli vielä paljon vähemmän tarkkoja mittareita. Nykyisissä päivityksissä ei esitetä uusia tapoja valvoa olemassa olevia mittareita sinänsä, mutta ne ehdottavat taktiikkaa "kuilun poistamiseksi markkinoiden edeltävän ja markkinoiden jälkeisen suorituskyvyn välillä".
"Menettelylliset muutokset" mittarin tarkkuussääntöihin
Vuonna 2016 päätetty pysyy enimmäkseen ennallaan - nämä uudet marraskuun 2018 muutokset eivät todellakaan paranna mittariemme käytännön tarkkuutta kotona tai kliinisissä olosuhteissa.
Sen sijaan FDA kertoo meille, että nämä uusimmat muutokset ovat suurelta osin "menettelyllisiä", ja niissä käsitellään sitä, kuinka valmistajien on seurattava prosessejaan ja vanteita, joiden on mentävä läpi saadakseen nämä mittarit ja nauhat markkinoille. FDA kertoo, että nämä muutokset tulivat alan toimijoiden erityisestä pyynnöstä, joiden mielestä vuoden 2016 asiakirja tarvitsi selvennystä.
"Molempien ohjeiden muutokset sisälsivät pieniä muutoksia", sanoi FDA: n lehdistövirkailija Stephanie Caccomo. "(Sisältää) sen selventämisen, että sponsorien on annettava perustelut mahdollisille tietojen poissulkemisille menetelmien vertailussa ja käyttäjien arvioinnissa, poistamalla erityiset esimerkit muutoksista ja erän vapauttamisperusteiden testauksesta ja lisäämällä ehdokaslaitteen vertailut testiolosuhteissa ehdokaslaitteeseen nimellisolosuhteissa tiettyihin tutkimuksiin. "
Toisin sanoen näkökohdat, jotka eivät tuota meille paljon hyötyä D-yhteisössä, kun käytämme näitä tuotteita omassa diabeteksemme päivittäin.
Aikaisempi, vuonna 2016 käyttöön otettu ohjeistus näistä kahdesta tuoteryhmästä tarjosi merkityksellisimmän muutoksen -
Jokaisen kohdalla tarkkuusstandardit edellyttävät, että verensokeritulokset ovat tietyn prosenttiosuuden tarkkuuden testaamisen vertailumenetelmästä; he saavat olla vain niin kaukana laboratorion sisäisen glukoositestin tuottamasta uber-tarkasta tuloksesta.
FDA kertoo meille, että he ottivat huomioon laajan palautteen saadakseen aikaan kompromissin, joka lisäisi tarkkuutta luomatta liikaa esteitä teollisuudelle.
"Valmistajilta saadun palautteen perusteella näiden nauhojen tarkkuuden lisääminen liikaa lisäisi niiden kustannuksia ja vähentäisi niiden saatavuutta potilaille", FDA: n tiedottaja Stephanie Caccomo sanoi. "Potilaiden palaute osoitti, etteivät he halunneet laitteen käytettävyyden vähentämistä (lisääntyneestä testausajasta, kasvaneesta näytemäärästä jne.) Pitääkseen yhtenäisen hinnoittelun nauhoille, joiden tarkkuutta on merkittävästi lisätty."
Hän lisäsi, että "tämä on merkittävä parannus tarkkuuteen verrattuna jopa viisi vuotta sitten markkinoituihin mittareihin", mutta FDA uskoo, että myös monien tänään markkinoilla olevien mittareiden pitäisi pystyä täyttämään nämä parannetut kriteerit.
Näiden kriteerien yksityiskohdat ovat seuraavat:
Kliiniset verensokerin seurantajärjestelmät (BGMS) -
- 95% arvoista on oltava +/- 12% sisällä verensokerien ollessa alle tai yli 75 mg / dl
- 98% sisällä +/- 15%
Vertailun vuoksi aiemmat säännöt vaativat 15 prosentin ja 20 prosentin tarkkuutta kaikilla alueilla. Vuoden 2014 alussa FDA oli ehdottanut tiukimman vaatimuksen tiukentamista +/- 10 prosenttiin, mutta mittareiden valmistajat ja kliinisen terveydenhuollon tarjoajat vastustivat, koska se voisi estää heitä joko tekemästä tai hankkimasta mittareita kohtuuhintaisesti. Joten sääntelyviranomaiset tapasivat keskellä 12%.
FDA: n tiedottaja kertoo meille, miksi luonnos ja lopullinen sääntö eroavat toisistaan, on "tasapainottaa kunkin väestön kliiniset tarpeet valmistajien kykyyn tuottaa laitteita, jotka täyttävät nämä tavoitteet".
Tässä on linkki FDA: n täydelliseen kliinisten mittareiden 43-sivuiseen ohjeeseen.
Henkilökohtaiset glukoosimittarit -
- 95% +/- 15% mittausalueella
- 99% +/- 20% mittausalueella
Aikaisemmissa säännöissä vaadittiin 20 prosentin tarkkuutta suhteessa useimpiin verensokeriarvoihin.
Vuodesta 2016 lähtien henkilökohtaisen käytön mittareissa on myös oltava "näkyvä varoitus" siitä, että niiden testiliuskoja (jotka mahdollistavat veren keräämisen "avoimessa" ympäristössä) ei ole tarkoitettu käytettäviksi kliinisissä olosuhteissa. Tämä johtuu sekä FDA: n että tautien torjuntakeskusten (CDC) pitkäaikaisesta huolestumisesta hepatiitti B: n ja muiden veren kautta tarttuvien tautien riskistä, ja se on tärkein syy viraston jakamaan säännöt kahteen eri ryhmään.
Tässä on linkki FDA: n 43-sivuiseen kotikäyttömittareita koskevaan asiakirjaan.
Muut uudet BG-mittarivaatimukset
Valmistusprosessi: FDA rajoitti tarkkuusstandardin lisäksi myös valmistajien erien julkaisumenetelmää - keräsi tietoja valmistajien sivustoista ja tuotannon laadusta. Tämä tapahtuu "tiedonkeruun ja paikan tarkastusten avulla", meille kerrotaan.
Merkinnät: Ehkä mikä tärkeintä, FDA on vaatinut uusia merkintätietoja testiliuskapulloista; Niiden on sisällettävä tiedot erästä / tuotannosta ja kuvaus suorituskyvystä (tarkkuustiedot) laatikon ulommassa etiketissä, jotta käyttäjät voivat verrata yhtä metriä toiseen.
Kolmannen osapuolen testiliuskat: Tärkeää on, että lopulliset säännöt lisäävät säännöksiä tuotemerkkien ulkopuolisille testiliuskanvalmistajille, joita on kritisoitu viime vuosina. Vaikka nämä nauhat ovat usein halvempia, niihin ei ole sovellettu samoja tarkkuusvaatimuksia kuin mittareihin - varsinkin kun tiettyjä tuotemerkkejä valmistetaan ulkomaille, eikä FDA pysty tarkastamaan tuotantolaitoksia kuten Yhdysvalloissa . FDA: n sääntöjen mukaan näiden valmistajien tulisi "varmistaa, että he ovat tietoisia mittarin suunnittelumuutoksista, koska tällaiset muutokset voivat vaikuttaa testiliuskan yhteensopivuuteen mittarin kanssa". Tähän on puututtava kolmannen osapuolen yrityksen 510 (k) -hakemuksessa, ja FDA suosittelee myös, että ne toimittavat kolmannen osapuolen nauhavalmistajan ja mittarinvalmistajan välisen sopimusasiakirjan.
Glukoosimittareiden markkinoiden jälkeinen seuranta
Viimeaikaisessa päivityksessään FDA ei sisältänyt uusia näkökohtia mittareiden ja nauhojen tutkimiseksi, kun ne ovat markkinoilla, lukuun ottamatta yleisiä säännöksiä ja käytäntöjä, joita sillä on jo tarkastusten ja laitosvaatimusten osalta.
Mutta virasto on tietoinen asiasta ja viittaa uusiin testiliuskaerän kriteereihin keinona käsitellä markkinoiden jälkeisiä huolenaiheita. FDA suosittelee, että 510 (k) -julkaisuissaan valmistajat antavat kuvauksen erän vapauttamisperusteista ja yhteenvedon näytteenottojärjestelmästä, jonka FDA aikoo tarkistaa uudelleen osana hyväksyntää.
"Pyrittäessä poistamaan ero markkinoinnin jälkeisen ja markkinoinnin jälkeisen suorituskyvyn sekä erojen välillä testiliuskojen välillä, testierien vapauttamisperusteiden pitäisi olla riittävät varmistamaan testiliuskojen tasainen laatu. Tämä tarjoaa suuremman johdonmukaisuuden erissä ja eri valmistajien keskuudessa sekä pidättelee markkinoiden jälkeisiä huonoja valmistuspäätöksiä ”, tiedottaja Caccomo kertoo.
Tämä on ollut viime vuosina kuuma aihe, joka on johtanut kehittyvän Diabetes Technology Society -valvontaohjelman käyttöön.
Noudattaminen on vapaaehtoista?
Epäilemättä uudet tarkemman tarkkuuden ohjeet ovat hyvä asia.
Ongelmana on, että vaikka lääketuotteiden on oltava FDA: n hyväksymiä, jotta ne tulevat markkinoille Yhdysvalloissa, nämä "ohjeet" eivät ole pakollisia, vaan pikemminkin "ei-sitovia" eli vapaaehtoisia. Tämä johtuu siitä, että FDA: n politiikassa todetaan, että sen ohjeet "eivät ole oikeudellisesti sitovia tietylle toimintatavalle ... (mutta) edustavat kuitenkin edelleen viraston parhaita neuvoja kyseessä olevasta asiasta niiden tekohetkellä" - oletettavasti viraston suojelemiseksi sotkeutua oikeusjuttuihin.
Mutta… uh.
Rehellisesti, mikä on järkeä, jos valmistajat voivat vain päättää olla noudattamatta näitä uusia sääntöjä? Voimme vain rikkoa sormiamme, että markkinapaine kannustaa myyjiä noudattamaan vaatimuksia. Huolimatta CGM: n ja automatisoidun D-tekniikan kasvavasta käytöstä, glukoosimittarit ja -nauhat ovat edelleen diabeteksen hallinnan "leipää ja voita" massoille (niin sanotusti), joten tarkkuuden varmistaminen on edelleen tärkeää.